S12 – Stabilité chimique : lecture de Lewis⚓︎
1️⃣ Les gaz nobles : modèles de stabilité⚓︎
Caractéristiques des gaz nobles⚓︎
Les gaz nobles (colonne 18 du tableau périodique) sont des éléments chimiquement inertes : ils ne réagissent quasiment pas avec les autres éléments.
| Gaz noble | Symbole | Z | e⁻ couche externe |
|---|---|---|---|
| Hélium | He | 2 | 2 |
| Néon | Ne | 10 | 8 |
| Argon | Ar | 18 | 8 |
Pourquoi sont-ils stables ?⚓︎
Leur couche électronique externe est complète : ils n'ont pas besoin de gagner, perdre ou partager des électrons.
2️⃣ La règle de l'octet (et du duet)⚓︎
Énoncé⚓︎
Les atomes cherchent à acquérir la configuration électronique stable des gaz nobles :
Comment atteindre cette stabilité ?⚓︎
| Méthode | Résultat | Exemple |
|---|---|---|
| Perdre des e⁻ | Formation d'un cation | Na → Na⁺ |
| Gagner des e⁻ | Formation d'un anion | Cl → Cl⁻ |
| Partager des e⁻ | Formation d'une liaison covalente | H₂, H₂O, CH₄ |
3️⃣ Les formules de Lewis⚓︎
Principe⚓︎
La représentation de Lewis permet de visualiser les électrons de valence d'un atome ou d'une molécule.
Conventions : - Un point (•) = 1 électron - Un trait (—) = 2 électrons (doublet)
Lewis des atomes courants⚓︎
| Atome | e⁻ de valence | Représentation |
|---|---|---|
| H | 1 | H• |
| C | 4 | 4 électrons autour |
| N | 5 | 1 doublet + 3 électrons |
| O | 6 | 2 doublets + 2 électrons |
| Cl | 7 | 3 doublets + 1 électron |
Types de doublets⚓︎
| Type | Description | Représentation | Exemple |
|---|---|---|---|
| Doublet liant | Partagé entre 2 atomes | — (trait) | Liaison O—H |
| Doublet non liant | Sur 1 seul atome | •• | Sur l'oxygène de H₂O |
Exemple : la molécule d'eau H₂O⚓︎
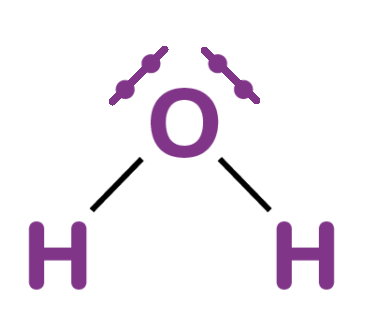
• 2 doublets liants (traits H—O) • 2 doublets non liants (sur O)
Vérification de l'octet : - Oxygène : 2 + 2 + 2 + 2 = 8 électrons ✓ - Hydrogène : 2 électrons chacun ✓ (règle du duet)
┌─────────────────────────────────────────────────────────────┐
│ │
│ 📌 À RETENIR : │
│ │
│ • Doublet LIANT = ENTRE deux atomes (liaison) │
│ • Doublet NON LIANT = SUR un seul atome │
│ │
└─────────────────────────────────────────────────────────────┘
4️⃣ Les radicaux : espèces instables⚓︎
Définition⚓︎
Un radical est une espèce chimique possédant un électron célibataire (non apparié).
Exemple : le radical hydroxyle HO•⚓︎
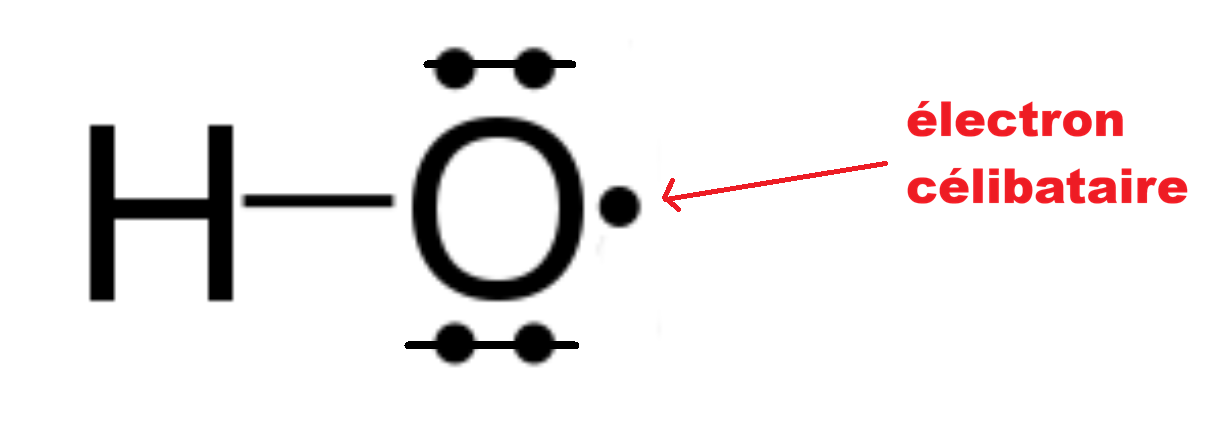
Électron célibataire → très réactif
L'oxygène n'a que 7 e⁻ au lieu de 8 → Le radical va "arracher" un électron à une molécule voisine
Les ROS (Espèces Réactives de l'Oxygène)⚓︎
| ROS | Formule | Source |
|---|---|---|
| Radical hydroxyle | HO• | UV, pollution |
| Anion superoxyde | O₂•⁻ | Métabolisme cellulaire |
| Peroxyde d'hydrogène | H₂O₂ | Métabolisme |
Conséquences sur la peau : - Attaque des lipides membranaires - Dégradation du collagène - Dommages à l'ADN - → Vieillissement cutané accéléré
5️⃣ Les liaisons fragiles O–O et S–S⚓︎
Liaison O–O (peroxyde)⚓︎
R — O — O — R
↑
Liaison FRAGILE
La liaison O–O a une énergie de liaison faible : elle se casse facilement.
| Composé | Formule | Utilisation |
|---|---|---|
| Eau oxygénée | H₂O₂ | Décoloration capillaire |
| Peroxyde de benzoyle | – | Actif anti-acné |
Liaison S–S (pont disulfure)⚓︎
R — S — S — R
↑
Liaison FRAGILE
La liaison S–S peut être réduite (cassée) ou oxydée (reformée).
| Structure | Localisation | Application |
|---|---|---|
| Cystine | Kératine du cheveu | Structure capillaire |
| Ponts S–S | Entre fibres de kératine | Permanente / défrisage |
6️⃣ Application : la permanente⚓︎
La permanente exploite la fragilité des liaisons S–S de la kératine.
┌─────────────────────────────────────────────────────────────────────┐
│ │
│ ÉTAPE 1 : RÉDUCTION │
│ ───────────────── │
│ Réducteur (acide thioglycolique) → CASSE les liaisons S–S │
│ Le cheveu devient MALLÉABLE │
│ │
│ ÉTAPE 2 : MISE EN FORME │
│ ─────────────────────── │
│ Bigoudis (boucles) ou lissage (défrisage) │
│ │
│ ÉTAPE 3 : OXYDATION │
│ ────────────────── │
│ Oxydant (H₂O₂) → REFORME les liaisons S–S │
│ Le cheveu GARDE sa nouvelle forme │
│ │
└─────────────────────────────────────────────────────────────────────┘
7️⃣ Les antioxydants : protection contre les radicaux⚓︎
Rôle des antioxydants⚓︎
Les antioxydants neutralisent les radicaux libres en leur donnant un électron, sans devenir eux-mêmes dangereux.
| Antioxydant | Type | Action |
|---|---|---|
| Vitamine C | Hydrosoluble | Neutralise les radicaux en milieu aqueux |
| Vitamine E | Liposoluble | Protège les membranes lipidiques |
| Polyphénols | Variable | Piègent les radicaux |
Synergie C + E⚓︎
La vitamine C régénère la vitamine E après que celle-ci a neutralisé un radical.
8️⃣ Électronégativité : un aperçu pour la suite⚓︎
Définition⚓︎
L'électronégativité (notée χ, « chi ») est la capacité d'un atome à attirer vers lui les électrons d'une liaison chimique.
Tendance dans le tableau périodique⚓︎
Valeurs utiles en cosmétique⚓︎
| Atome | χ (Pauling) | Commentaire |
|---|---|---|
| H | 2,2 | Référence |
| C | 2,5 | Peu électronégatif |
| N | 3,0 | Électronégatif |
| O | 3,4 | Très électronégatif |
| F | 4,0 | Le plus électronégatif |
| S | 2,6 | Proche du carbone |
| Cl | 3,2 | Électronégatif |
💡 En S13, nous verrons comment la DIFFÉRENCE d'électronégativité entre deux atomes crée une liaison polarisée, ce qui explique pourquoi certaines molécules cosmétiques sont solubles dans l'eau et d'autres dans l'huile.
📌 À retenir pour l'E2⚓︎
Règles de stabilité⚓︎
| Règle | Application |
|---|---|
| Règle de l'octet | 8 e⁻ sur la couche externe = stable |
| Règle du duet | 2 e⁻ pour l'hydrogène |
| Gaz nobles | Configuration idéale (couche pleine) |
Signes d'instabilité⚓︎
| Signe | Conséquence |
|---|---|
| Électron célibataire | Radical (très réactif) |
| Liaison O–O | Fragile (se casse facilement) |
| Liaison S–S | Fragile (permanente, défrisage) |
Vocabulaire à maîtriser⚓︎
| Terme | Définition |
|---|---|
| Doublet liant | 2 e⁻ partagés entre 2 atomes (liaison) |
| Doublet non liant | 2 e⁻ sur un seul atome |
| Radical | Espèce avec un e⁻ célibataire |
| ROS | Espèces réactives de l'oxygène (radicaux) |
| Antioxydant | Molécule qui neutralise les radicaux |
🔗 Lien avec la suite de la progression⚓︎
| Séance | Réinvestissement |
|---|---|
| S13 | Polarité et interactions (liaisons H, Van der Waals) |
| S19 | Fonctions organiques (alcools, peroxydes, thiols) |
| S26 | Stabilité des cosmétiques, facteurs de dégradation |