S12 – Stabilité chimique : lecture de Lewis 📝⚓︎
Gaz nobles – Règle de l'octet – Doublets – Radicaux – Liaisons fragiles
En BTS MECP, on attend des réponses rédigées, justifiées et utilisant un vocabulaire scientifique précis. Comprendre la stabilité des molécules permet d'anticiper la conservation des cosmétiques et l'action des actifs.
🎯 Objectifs de la séance⚓︎
À l'issue de cette séance, vous serez capables de :
- expliquer pourquoi les gaz nobles sont stables
- appliquer la règle de l'octet (ou du duet)
- lire une formule de Lewis (doublets liants et non liants)
- identifier un radical (électron célibataire)
- repérer les liaisons fragiles (O–O, S–S)
- relier la structure d'une molécule à sa stabilité
🧴 Pourquoi c'est important pour votre métier ?⚓︎
En institut ou en laboratoire cosmétique, vous serez amené(e) à :
- Comprendre la conservation des produits : les molécules instables se dégradent plus vite
- Interpréter l'action des actifs : peroxydes (décoloration), thiols (permanente)
- Conseiller sur les antioxydants : ils neutralisent les radicaux libres responsables du vieillissement
- Lire les fiches techniques : identifier les composés sensibles à l'oxydation
💡 Savez-vous que la vitamine C (acide ascorbique) s'oxyde très vite et jaunit ? C'est parce que sa structure contient des liaisons fragiles. Les cosmétiques utilisent des formes stabilisées comme l'Ascorbyl Glucoside !
👉 Cette séance vous permettra de lire une formule de Lewis et d'en déduire si une molécule est stable ou fragile.
🧴 Situation professionnelle⚓︎
Vous travaillez au service R&D d'un laboratoire cosmétique.
Le formulateur vous montre deux actifs anti-âge : - L'acide ascorbique (vitamine C pure) – se dégrade en quelques semaines - L'Ascorbyl Tetraisopalmitate – stable plusieurs mois
« Pourquoi ces deux molécules ont-elles des stabilités si différentes alors qu'elles contiennent toutes les deux de la vitamine C ? »
Pour répondre, vous devez comprendre la structure chimique et identifier les zones de fragilité.
📄 Documents fournis⚓︎
Document 1 – Les gaz nobles : modèles de stabilité⚓︎
Les gaz nobles (colonne 18 du tableau périodique) sont des éléments chimiquement inertes : ils ne réagissent quasiment pas avec les autres éléments.
| Gaz noble | Symbole | Z | Configuration électronique | e⁻ couche externe |
|---|---|---|---|---|
| Hélium | He | 2 | K² | 2 |
| Néon | Ne | 10 | K² L⁸ | 8 |
| Argon | Ar | 18 | K² L⁸ M⁸ | 8 |
| Krypton | Kr | 36 | K² L⁸ M¹⁸ N⁸ | 8 |
Pourquoi sont-ils stables ? Leur couche électronique externe est complète : - 2 électrons pour l'hélium (couche K pleine) - 8 électrons pour les autres (couche externe pleine)
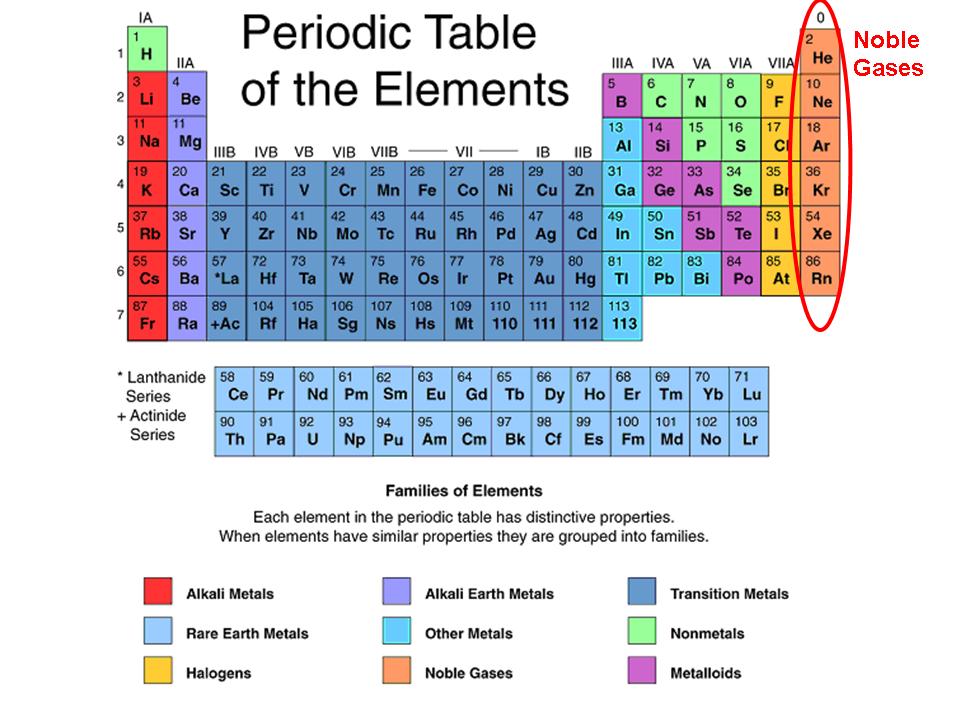
Gaz nobles : couche externe pleine → stabilité
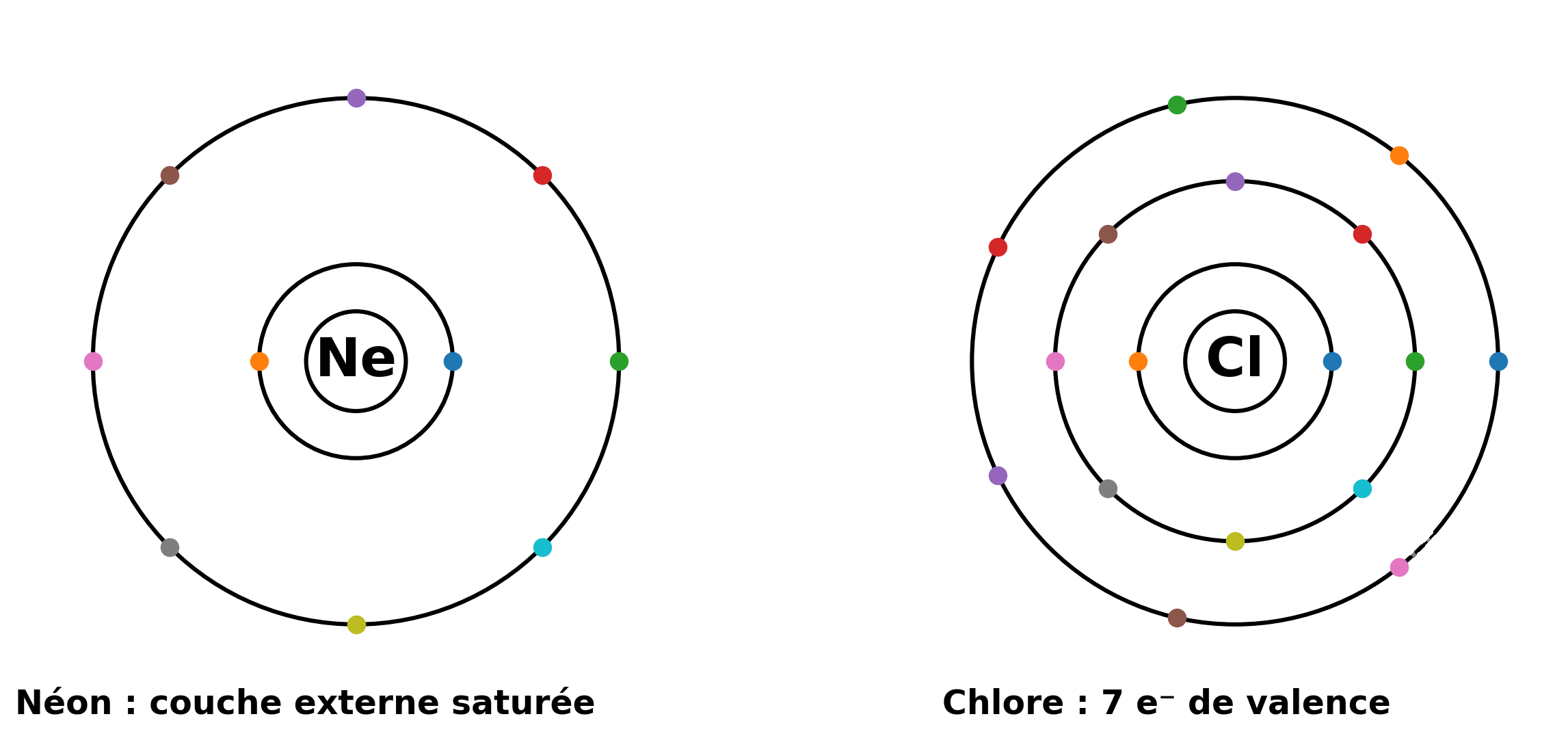
Ne : couche externe pleine ; Cl : 7 e⁻ de valence → tendance à compléter
Document 2 – La règle de l'octet (et du duet)⚓︎
Les atomes cherchent à acquérir la configuration électronique stable des gaz nobles :
Comment atteindre cette stabilité ? - En perdant ou gagnant des électrons → formation d'ions (S11) - En partageant des électrons → formation de liaisons covalentes
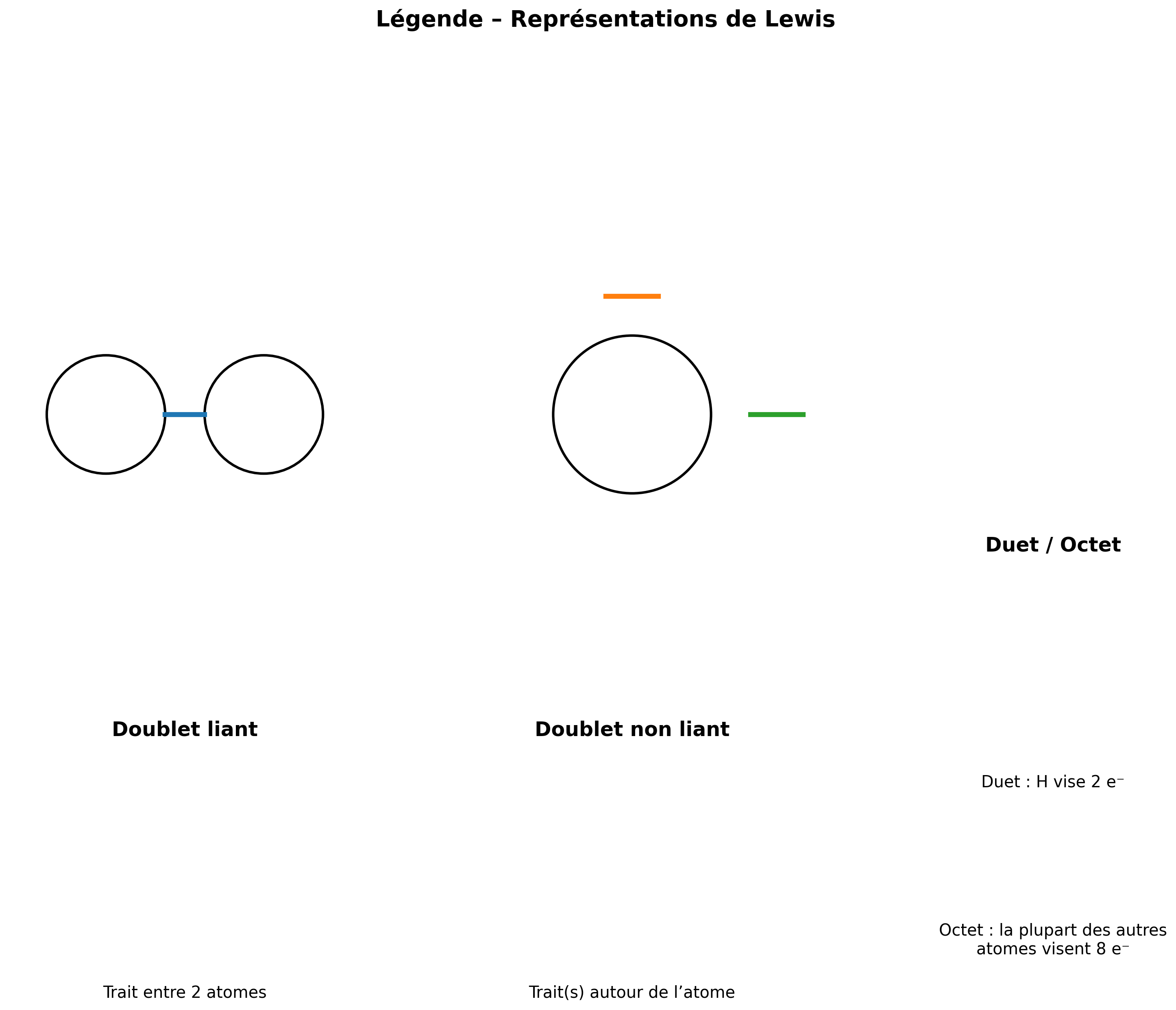
Repères : doublets liants / non liants
Document 3 – Les formules de Lewis⚓︎
La représentation de Lewis permet de visualiser les électrons de valence d'un atome ou d'une molécule.
Conventions : - Un point (•) représente 1 électron - Un trait (—) représente 2 électrons (un doublet)
Lewis des atomes courants :
| Atome | e⁻ de valence | Représentation de Lewis |
|---|---|---|
| H | 1 | H• |
| C | 4 | C avec 4 points autour |
| N | 5 | N avec 1 doublet + 3 points |
| O | 6 | O avec 2 doublets + 2 points |
| Cl | 7 | Cl avec 3 doublets + 1 point |
Représentation simplifiée :
Hydrogène Carbone Azote Oxygène Chlore
• __ • __
H• •C• •N• |O| |Cl|
• • • •
(1 e⁻) (4 e⁻) (5 e⁻) (6 e⁻) (7 e⁻)
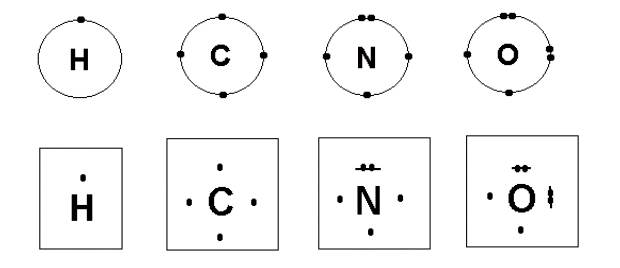
Exemples de Lewis d’atomes et molécules
Document 4 – Doublets liants et non liants⚓︎
Quand deux atomes mettent en commun des électrons, ils forment une liaison covalente.
| Type de doublet | Description | Représentation |
|---|---|---|
| Doublet liant | Paire d'électrons partagée entre 2 atomes | — (trait) |
| Doublet non liant | Paire d'électrons appartenant à 1 seul atome | •• ou — sur l'atome |
Exemple : la molécule d'eau H₂O
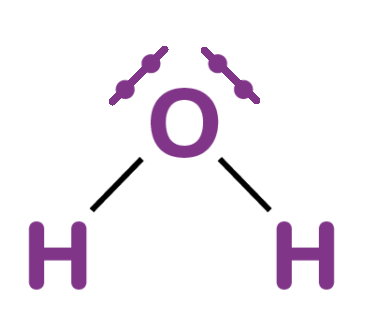
• 2 doublets liants (traits H—O) • 2 doublets non liants (sur O)
Vérification de l'octet : - Oxygène : 2 + 2 + 2 + 2 = 8 électrons ✓ - Hydrogène : 2 électrons chacun ✓ (règle du duet)
Exemple : la molécule de dioxygène O₂

• 1 double liaison (4 e⁻ partagés) • 2 doublets non liants sur chaque O
Exemple : la molécule de dichlore Cl₂
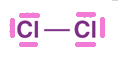
Document 5 – Indices d'instablilité⚓︎
A) Radical (électron célibataire)⚓︎
Un radical est une espèce chimique possédant un électron célibataire (non apparié).
Exemple : le radical hydroxyle HO•
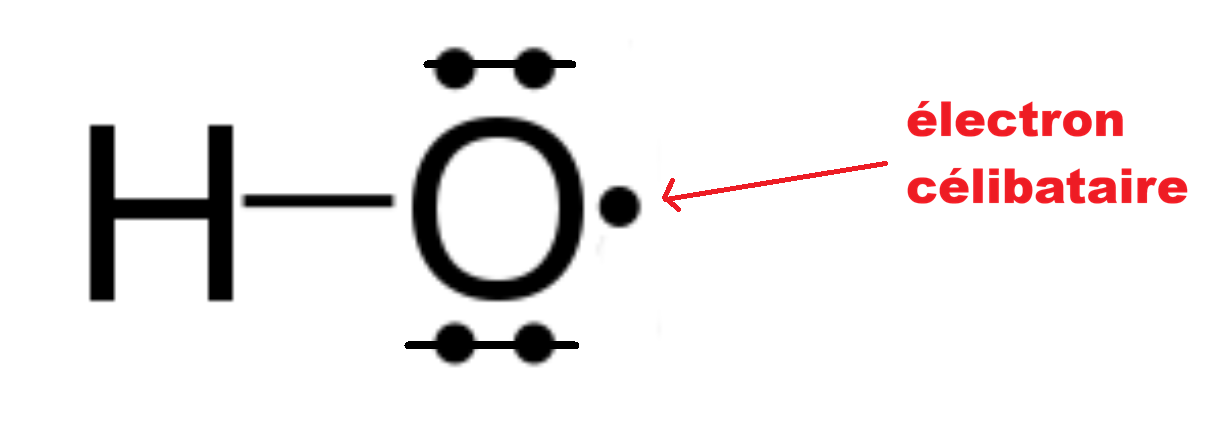
Électron célibataire → très réactif
L'oxygène n'a que 7 e⁻ → il lui en manque 1 pour l'octet → Il va "arracher" un électron à une molécule voisine
Les ROS (Reactive Oxygen Species) – Espèces Réactives de l'Oxygène :
| ROS | Formule | Origine | Effet sur la peau |
|---|---|---|---|
| Radical hydroxyle | HO• | UV, pollution | Très agressif |
| Anion superoxyde | O₂•⁻ | Métabolisme | Stress oxydatif |
| Peroxyde d'hydrogène | H₂O₂ | Métabolisme | Précurseur de HO• |
⚠️ Les ROS sont responsables du vieillissement cutané : ils attaquent les lipides membranaires, les protéines (collagène) et l'ADN des cellules.
B) Lacune électronique (octet incomplet)⚓︎
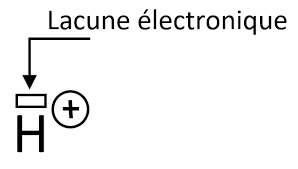
Octet incomplet → tendance à réagir
Document 6 – Les liaisons fragiles O–O et S–S⚓︎
Certaines liaisons sont plus faciles à casser que d'autres. Les liaisons O–O (peroxyde) et S–S (pont disulfure) sont particulièrement fragiles.
Liaison O–O (peroxyde) :
R — O — O — R
↑
Liaison FRAGILE
(énergie de liaison faible)
| Composé | Formule | Utilisation cosmétique |
|---|---|---|
| Eau oxygénée | H₂O₂ | Décoloration capillaire |
| Peroxyde de benzoyle | C₁₄H₁₀O₄ | Actif anti-acné |
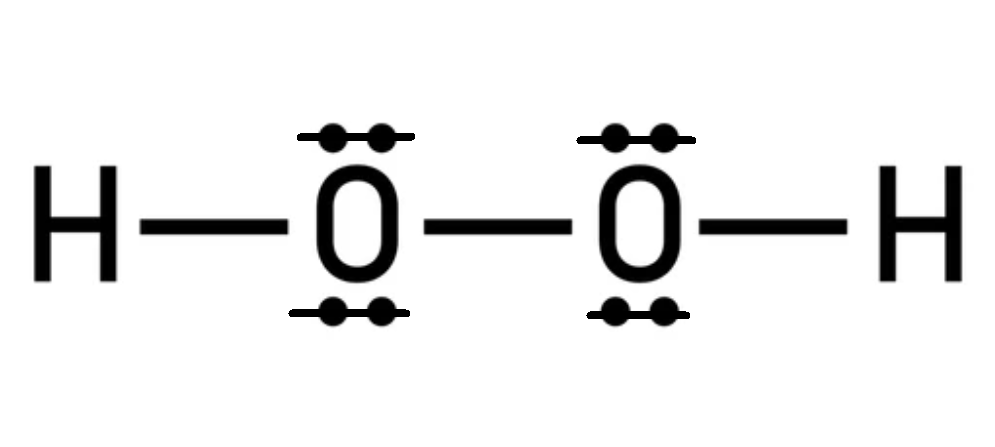
La liaison O–O est plus fragile → peut générer des espèces réactives
Liaison S–S (pont disulfure) :
R — S — S — R
↑
Liaison FRAGILE
(peut être réduite ou oxydée)
| Structure | Localisation | Application |
|---|---|---|
| Cystine | Kératine du cheveu | Donne sa solidité au cheveu |
| Ponts S–S | Entre les fibres | Modifiés par permanente/défrisage |

Ponts S–S : structure de la kératine (cheveu)
Document 7 – La permanente : exploitation des liaisons S–S⚓︎
La permanente et le défrisage exploitent la fragilité des liaisons S–S de la kératine.
Étapes :
CHEVEU NATUREL RÉDUCTION MISE EN FORME OXYDATION
~~~S—S~~~ → ~~~SH HS~~~ → Bigoudis/lissage → ~~~S—S~~~
Acide thioglycolique Nouvelle forme Eau oxygénée
(casse les S—S) du cheveu (reforme les S—S)
- Réducteur (ex : acide thioglycolique) → casse les liaisons S–S
- Mise en forme → le cheveu est malléable
- Oxydant (ex : H₂O₂) → reforme les liaisons S–S dans la nouvelle position
- Résultat → le cheveu garde sa nouvelle forme (boucles ou lissage)
🔬 Travail 1 – Stabilité et gaz nobles⚓︎
1.1 – Les gaz nobles⚓︎
À partir du Document 1, répondez aux questions :
1. Quelle est la particularité de la couche externe des gaz nobles ?
2. Combien d'électrons possède la couche externe du néon ? De l'argon ?
3. Pourquoi les gaz nobles sont-ils chimiquement inertes (stables) ?
1.2 – La règle de l'octet⚓︎
Complétez les phrases :
1. Pour être stable, un atome doit avoir _ électrons sur sa couche externe.
2. L'hydrogène fait exception : il suit la règle du _ (_ électrons).
3. Un atome peut atteindre la stabilité en formant des _ covalentes (partage d'électrons).
📊 Travail 2 – Lire une formule de Lewis⚓︎
🎯 Compétence E2 : Mobiliser – Identifier les doublets sur une formule.
2.1 – Identifier les doublets⚓︎
Pour chaque molécule, comptez les doublets liants et non liants :
Molécule 1 : Méthane CH₄
H
|
H — C — H
|
H
- Nombre de doublets liants : _
- Nombre de doublets non liants : _
Molécule 2 : Ammoniac NH₃
_
N
/ | \
H H H
- Nombre de doublets liants : _
- Nombre de doublets non liants : _
Molécule 3 : Dioxyde de carbone CO₂
- -
O == C == O
- -
- Nombre de doublets liants : _
- Nombre de doublets non liants : _
2.2 – Vérifier l'octet⚓︎
Pour la molécule d'eau H₂O, vérifiez que chaque atome respecte la règle de l'octet (ou du duet) :
-
H — O — H
-
- Oxygène : _ doublets × 2 = _ électrons → Octet respecté ? ☐ Oui ☐ Non
- Hydrogène : _ électrons → Duet respecté ? ☐ Oui ☐ Non
🧪 Travail 3 – Radicaux et liaisons fragiles⚓︎
🎯 Compétence E2 : Interpréter – Identifier les zones d'instabilité.
3.1 – Identifier un radical⚓︎
Parmi les espèces suivantes, identifiez celles qui sont des radicaux (électron célibataire) :
| Espèce | Formule de Lewis | Radical ? |
|---|---|---|
| Eau | H—O—H avec 2 doublets sur O | ☐ Oui ☐ Non |
| Radical hydroxyle | H—O• avec 1 doublet et 1 e⁻ seul sur O | ☐ Oui ☐ Non |
| Chlorure | Cl⁻ avec 4 doublets | ☐ Oui ☐ Non |
| Radical méthyle | •CH₃ | ☐ Oui ☐ Non |
3.2 – Liaisons fragiles⚓︎
Sur les formules suivantes, entourez la liaison fragile :
Peroxyde d'hydrogène H₂O₂ :
- -
H — O — O — H
- -
Type de liaison fragile : _
Cystine (acide aminé soufré) :
HOOC—CH—CH₂—S—S—CH₂—CH—COOH
| |
NH₂ NH₂
Type de liaison fragile : _
3.3 – Question de réflexion⚓︎
Pourquoi les radicaux libres (ROS) sont-ils dangereux pour la peau ? Utilisez les termes : électron célibataire, réactif, molécules biologiques.
📈 Travail 4 – Applications cosmétiques⚓︎
🎯 Compétence E2 : Argumenter – Relier structure et stabilité.
4.1 – La décoloration capillaire⚓︎
L'eau oxygénée (H₂O₂) est utilisée pour décolorer les cheveux.
1. Quelle liaison fragile contient H₂O₂ ?
2. Quand cette liaison se casse, quels radicaux peuvent se former ?
3. Comment ces radicaux agissent-ils sur la mélanine (pigment du cheveu) ?
4.2 – La permanente⚓︎
Expliquez en 4-5 lignes le principe chimique de la permanente en utilisant les termes : liaison S–S, réducteur, oxydant, kératine.
4.3 – Conservation des cosmétiques⚓︎
Un sérum contient de la vitamine C pure (acide ascorbique). Après quelques semaines, il devient jaune-brun.
1. Ce changement de couleur indique-t-il une réaction chimique ? ☐ Oui ☐ Non
2. Quel type d'espèces chimiques a probablement attaqué la vitamine C ?
3. Proposez deux solutions pour améliorer la stabilité de ce sérum :
- Solution 1 :
- Solution 2 :
🔄 Travail 5 – Exercice de synthèse (niveau E2)⚓︎
🎯 Compétence E2 : Argumenter et Communiquer
Situation professionnelle⚓︎
Le laboratoire compare deux actifs anti-âge :
| Actif | Structure | Stabilité |
|---|---|---|
| Rétinol (vitamine A) | Contient plusieurs doubles liaisons C=C | Se dégrade rapidement à la lumière et à l'air |
| Rétinyl Palmitate | Rétinol estérifié (liaison ester protectrice) | Plus stable, libère le rétinol lentement |
Questions⚓︎
5.1 Pourquoi le rétinol est-il instable ? Quelle partie de sa structure est fragile ?
5.2 Comment l'estérification (Rétinyl Palmitate) améliore-t-elle la stabilité ?
5.3 En tant que formulateur, quel actif choisiriez-vous pour un sérum de jour ? Justifiez en 3-4 lignes.
🚀 Travail 6 – Approfondissement (pour aller plus loin)⚓︎
⚡ Ce travail est facultatif.
Les antioxydants : protecteurs contre les radicaux⚓︎
Les antioxydants sont des molécules capables de neutraliser les radicaux libres en leur donnant un électron, sans devenir eux-mêmes des radicaux dangereux.
| Antioxydant | Source | Mécanisme |
|---|---|---|
| Vitamine C | Agrumes, kiwi | Donne un électron au radical |
| Vitamine E | Huiles végétales | Protège les lipides membranaires |
| Polyphénols | Thé vert, raisin | Piègent les radicaux |
| Coenzyme Q10 | Mitochondries | Régénère la vitamine E |
Questions⚓︎
1. Expliquez comment un antioxydant peut neutraliser un radical sans créer de réaction en chaîne.
2. Pourquoi associe-t-on souvent vitamine C et vitamine E dans les soins anti-âge ?
✍️ Synthèse personnelle (entraînement E2 – 5 à 7 lignes)⚓︎
🎯 Compétence E2 : Communiquer
Rédigez un court paragraphe expliquant ce qu'est une molécule stable, comment reconnaître une zone de fragilité sur une formule de Lewis, et pourquoi c'est important en cosmétique.
Votre synthèse doit contenir : - La règle de l'octet et son lien avec la stabilité - La définition d'un radical - Les liaisons fragiles O–O et S–S - Un exemple d'application cosmétique
Mots obligatoires à placer : octet – doublet – radical – électron célibataire – liaison fragile – stabilité – antioxydant
🏆 Mes réussites aujourd'hui⚓︎
Avant de passer à l'auto-évaluation, prenez un moment pour reconnaître vos progrès !
Cochez ce que vous avez réussi à faire :
| Réussite | ✓ |
|---|---|
| J'ai compris pourquoi les gaz nobles sont stables | ☐ |
| Je sais appliquer la règle de l'octet | ☐ |
| Je sais identifier les doublets liants et non liants | ☐ |
| Je sais reconnaître un radical (électron célibataire) | ☐ |
| Je connais les liaisons fragiles O–O et S–S | ☐ |
| Je comprends le lien entre structure et stabilité | ☐ |
💡 Chaque case cochée est une victoire ! Vous savez maintenant "lire" une molécule pour anticiper sa stabilité.
✅ Auto-évaluation⚓︎
Avant de rendre votre travail, vérifiez :
| Critère | ✓ |
|---|---|
| Je connais la règle de l'octet (8 e⁻) et du duet (2 e⁻ pour H) | ☐ |
| Je sais distinguer doublet liant (entre 2 atomes) et non liant (sur 1 atome) | ☐ |
| Je sais qu'un radical possède un électron célibataire | ☐ |
| Je connais les liaisons fragiles : O–O et S–S | ☐ |
| Je comprends le lien avec la conservation des cosmétiques | ☐ |
| J'ai rédigé ma synthèse avec les mots obligatoires | ☐ |
🔗 Pour la suite de la progression⚓︎
Dans les séances suivantes, vous découvrirez : - S13 : Interactions moléculaires et pénétration cutanée - S19 : Fonctions organiques (alcools, peroxydes, thiols...)
🔧 Outils méthodologiques associés⚓︎
➡️ Fiche méthode 01 – Justifier une réponse scientifique (O.A.C.J.)
➡️ Fiche méthode 06 – Lire une formule de Lewis
📺 Pour réviser en vidéo⚓︎
🎬 Les formules de Lewis – Lumni – 5 min Comprendre les représentations de Lewis.
🎬 Les radicaux libres et le vieillissement – 4 min Pourquoi les radicaux libres abîment la peau.
🎬 La permanente : chimie du cheveu – 6 min Rôle des liaisons S–S dans la structure capillaire.
💡 Conseil : Ces notions sont fondamentales pour comprendre la stabilité des actifs cosmétiques !